质粒存在于许多细菌以及酵母菌等生物中,是细胞染色体外能够自主复制的很小的环状DNA分子。在基因工程中,质粒制备可将质粒作为目的基因的载体,在新的宿主生物体中正常表达。质粒DNA可以作为疫苗或治疗性药物单独使用,或在病毒载体生产中作为病毒包装的原料。
质粒制备的步骤

质粒制备流程图
质粒制备常见问题
Q:转化后克隆数量少
A:可以设置阴性和阳性对照。克隆过程中,阴性对照-空载长出菌落,判定可能是酶切不完全导致,阳性对照不出斑,可能是转化实验的操作出现问题。感受态细胞切勿反复冻融,且热激时间一定要精准到秒,同时正确使用抗生素或其他筛选标记。
Q:菌落太多但假阳性率高,挑不到正确克隆
A:菌落PCR鉴定引物需跨区域设计,一条引物设计在载体上,另外一条在目标片段上。如此可避免假阳性克隆又筛除反向插入片段,还可以通过提取质粒酶切跑胶进一步排除错误克隆。
Q:大肠杆菌老化
A:建议涂布平板培养后,重新挑选新菌落进行液体培养。
Q:质粒未全部溶解
A:洗脱溶解质粒时,可适当加温或延长溶解时间。
Q:质粒提取不成功
A:裂解时间过长,一般不应超过5分钟。吸附时间,溶解时间不够都会导致质粒DNA提取实验失败。
质粒制备|豪利777生物
豪利777生物拥有完善的质粒制备生产线,确保提供无RNA污染、无基因组污染的高质量无菌质粒,可将内毒素含量控制在较低水平(< 100EU/mg、<30EU/mg、<5EU/mg,供选择)。另外我们还提供序列验证、限制酶酶切和内毒素分析等服务,满足各领域客户多样化的下游应用,如转染、抗体制备,疫苗和基因治疗研究等。
案例分享——转染级质粒制备
将质粒转化后挑取单克隆菌落进行培养,抽提菌液进行酶切及测序验证,对符合要求的质粒进行大批量接菌抽提,之后对各批次抽提质粒进行酶切验证,无误后混合所有抽提质粒,最后对大抽质粒进行去内毒素处理,48h细菌检测如图1所示。
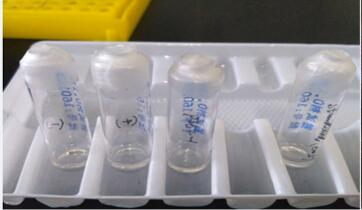
图1 内毒素检测
内毒素检测结果为阴性对照不凝固,阳性对照凝固,测试稀释样品不凝固,标准品不凝固,证明去内毒素处理成功。
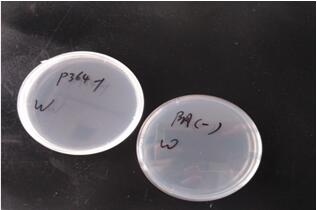
经过细菌检测结果比对,48h无抗培养基均不长斑,通过无菌检测。
 Syno®C 引物合成
Syno®C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno®GS 基因合成
Syno®GS 基因合成 载体构建
载体构建 高通量及DNA文库构建
高通量及DNA文库构建 CRISPR基因编辑平台
CRISPR基因编辑平台 病毒包装
病毒包装 基因测序及分析
基因测序及分析 重组蛋白表达平台
重组蛋白表达平台 抗体工程平台
抗体工程平台 多肽服务
多肽服务 生物信息学分析与设计
生物信息学分析与设计 CRISPR文库
CRISPR文库 ProXpress蛋白快速检测
ProXpress蛋白快速检测 CRISPR 质粒
CRISPR 质粒





















